Los enormes avances en la tecnología médica han llevado a la implantación de dispositivos neurológicos cada vez más avanzados, como estimuladores profundos del cerebro, del nervio vago y de la médula espinal. Elon Musk Neuralinkuna interfaz inalámbrica cerebro-computadora (BCI), es uno de los dispositivos más conocidos. Porcelana presentó recientemente su propio implante BCI, lo que indica que está alcanzando rápidamente a los EE. UU. en el espacio neurotecnológico.

Los dispositivos neurotecnológicos implantados han mejorado la calidad de vida de las personas que padecen enfermedades neurológicas. Pero, dada la velocidad de avance que estamos viendo actualmente, ¿qué sucede cuando la neurotecnología implantada se vuelve rápidamente obsoleta? ¿O ya no recibe soporte de mantenimiento de su fabricante (piense en Windows retirando el soporte para versiones obsoletas de su sistema operativo)? ¿Se puede eliminar y, de ser así, quién paga por ello?
Todo se reduce a esto: ¿Deberían existir protecciones para cubrir estas situaciones? Algunos argumentan que sí, deberían serlo. En un artículo publicado recientemente, un estudio dirigido por investigadores del Instituto Norman Fixel para Enfermedades Neurológicas en Florida, EE.UU., propuso una definición formal de «abandono de dispositivos neurológicos implantados» que, según afirman, es importante para desarrollar directrices, políticas y leyes relacionadas a dispositivos neurotecnológicos implantables.
Neurotech implantado como parte de un ensayo clínico
En 2020, Medicina de la naturaleza informó la historia de la mujer australiana Rita Leggett, que había recibido un implante cerebral experimental para tratar su epilepsia. Implantado como parte de un ensayo clínico, el dispositivo funcionó para Leggett: dejó de tener convulsiones. Sin embargo, a mitad del juicio, Neurovistala empresa que fabricó el dispositivo, cerró después de que los inversores se pusieron nerviosos acerca de proporcionar respaldo financiero a una tecnología tan invasiva.
Como la empresa ya no estaba operativa, no había forma de controlar el dispositivo. Estaba, literalmente, muerta en la cabeza de Leggett (bueno, no del todo: la batería debía durar tres años). Su marido se ofreció a comprar el dispositivo de NeuroVista, pero fue rechazado debido a sus componentes patentados. Su única opción era que le quitaran el dispositivo o lo «explantaran».
Según Frederic Gilbert, profesor asociado de la Universidad de Tasmania que se especializa en la ética de la neurotecnología y fue entrevistado para el Naturaleza Medicamento En este artículo, retirar un dispositivo puede equivaler a retirar el tratamiento. Gilbert dijo que eso se debe a que estos dispositivos pueden afectar profundamente la identidad de un paciente. La angustia causada por la retirada del dispositivo puede ser directamente proporcional a la eficacia de la tecnología.
Los autores del estudio actual formaron la opinión de que, a primera vista, el fracaso del ensayo clínico no fue un abandono de un dispositivo neurotecnológico principalmente porque el fracaso puede deberse a preocupaciones de seguridad o a la falta de efecto terapéutico. Sin embargo, dijeron que es esencial que quienes realizan un ensayo clínico cumplan tres criterios para permanecer en el lado «correcto» del abandono. En primer lugar, se debe informar a los participantes del estudio sobre la posibilidad de que se interrumpa el ensayo y que se les asignará a los brazos de tratamiento o control de la investigación. En segundo lugar, se debe notificar a los participantes si se suspenderá un ensayo y cuándo. Finalmente, se debe proporcionar a los participantes recursos para otras terapias que cumplan con los estándares de atención aceptados.
Por supuesto, además de la cuestión de que los ensayos finalicen prematuramente, está la cuestión de qué sucede con un implante neurotecnológico cuando un ensayo llega a su conclusión natural. En esa situación, generalmente se ofrece a los participantes la extracción del dispositivo. Sin embargo, normalmente ocurre después de que los investigadores se han puesto en contacto con sus compañías de seguros de salud públicas o privadas para ver si cubrir el costo. No existen pautas actuales claras sobre si un implante permanece puesto o se retira.
El colapso de las empresas de neurotecnología
Se espera que el mercado mundial de productos neurotecnológicos alcance 17.100 millones de dólares en 2026. Sin embargo, eso no garantiza que las empresas que fabrican estos productos se mantengan a flote. NeuroVista no es la única empresa de neurotecnología que ha cerrado sus puertas a los consumidores.
En 2019, Autonomic Technologies (ATI) suspendió sus operaciones luego de pruebas exitosas controladas con placebo de su estimulador, que trata las cefaleas en racimos. Es cierto que la empresa cerró debido a un fraude regulatorio, pero el resultado de la más de 700 Las personas que usaban el dispositivo eran iguales: no podían acceder al software propietario necesario para recalibrarlo y mantener su efectividad. Por suerte, Unity HA adquirió la propiedad intelectual de ATI y, en 2022, se le concedió Designación de dispositivo innovador por la FDA.

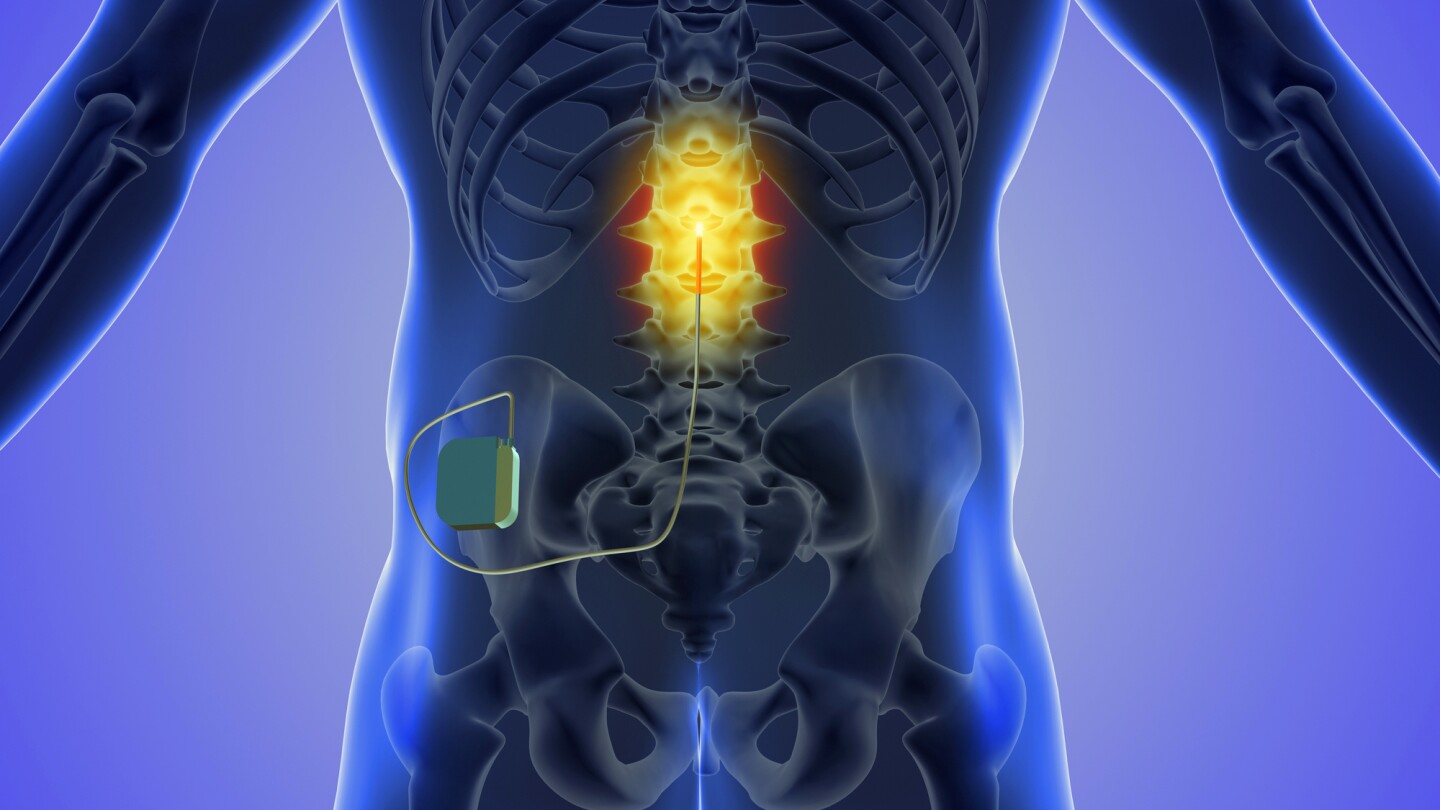
Nuvectra, fabricante de un estimulador de médula espinal para el dolor crónico, declarado en bancarrota en 2019. El mismo año, la empresa de visión artificial Second Sight comenzó a perder dinero y avisó a los implantados que estaban detener la producción de sus implantes de retina para centrarse en implantes cerebrales para restaurar la visión. A principios de 2020, el director ejecutivo y el director de investigación y desarrollo dimitieron repentinamente, la mayoría de los empleados fueron despedidos y la empresa comenzó a subastar sus activos físicos, dejando a unas 350 personas equipadas con un implante Second Sight preguntándose qué estaba pasando. La empresa se fusionó con Nano Precision Medicine (NPM) poco después. A mediados de 2020, otro fabricante de estimuladores de médula espinal, Stimware, retiró todos sus dispositivos y, en 2022, se declaró en quiebra. Seguramente habrá más.
Cuando empresas como estas quiebran, los implantes que crearon normalmente se dejan en su lugar. En la mayoría de los casos, la explantación se considera demasiado costosa, demasiado arriesgada o simplemente innecesaria. Entonces, para las personas con afecciones neurológicas, todo es volver a la mesa de dibujo, aunque con una pieza adicional de hardware (inútil).
Si tienen suerte, podrán encontrar un dispositivo de reemplazo. Según un artículo publicado en Naturaleza En 2022, reemplazar implantes obsoletos como el estimulador de médula espinal de Nuvectra requerirá una cirugía cuya recuperación llevará semanas. Además, es caro. La cirugía y el dispositivo de sustitución le costarán unos 40.000 dólares. Y eso suponiendo que haya un dispositivo de reemplazo disponible.
Longevidad del dispositivo: quitar o no quitar
Como ya se ha mencionado, un dispositivo neurotecnológico considerado de vanguardia hoy puede no serlo mañana. Estos dispositivos tienen una fecha de vencimiento incorporada, momento en el cual dejan de ser funcionales y efectivos sin mantenimiento y soporte continuos.
En el verano de 2020, Elon Musk compartió una actualización del progreso del implante Neuralink. Al describir el dispositivo como un “Fitbit en tu cráneo”, Musk se mostró característicamente indiferente al describir el proceso de inserción que imaginaba utilizar eventualmente en humanos.
«Básicamente, se abre un trozo de cráneo», dijo. “Se retira aproximadamente un trozo de cráneo del tamaño de una moneda y luego el robot inserta los electrodos… Luego, el dispositivo reemplaza la porción de cráneo que se extrajo. Y básicamente lo cerramos con superpegamento, que es la forma en que se cierran muchas heridas. Y luego puedes simplemente caminar justo después. Es genial.»
Sí, genial. Pero lo que fue más interesante fue la sección de la presentación que se refería a la cerda Dorothy, que solía tener un Neuralink. Musk dijo que retirar el implante de Dorothy demostraba la «reversibilidad» del dispositivo.
«Lo que Dorothy ilustra es que puedes ponerte el Neuralink, quitártelo y ser feliz, saludable e indistinguible de un cerdo normal», dijo Musk.
Eso es todo lo que Musk ofreció sobre la eliminación del dispositivo. Nada sobre sus riesgos. La actualización completa del progreso de Neuralink 2020 está disponible a continuación.
Actualización de progreso de Neuralink, verano de 2020
Desde entonces, la compañía de implantes cerebrales de Musk dejó de lado los cerdos y comenzó a reclutar para su primer ensayo en humanos. Pero primero tuvo que luchar contra la FDA para obtener su aprobación. Reuters informó en 2023 que la agencia rechazó una solicitud de aprobación de prueba por motivos de seguridad del paciente, citando grandes preocupaciones sobre, entre otras cosas, cómo se podría extraer el dispositivo sin dañar el tejido cerebral. almizcle tiene su aprobación ahorapor lo que la FDA parece estar satisfecha.
Es difícil encontrar comentarios de expertos sobre si la eliminación de Neuralink (u otro implante cerebral) dañará o no el cerebro. Para ser justos con Musk, sin sujetos humanos, puede resultar injusto especular en este momento. Pero, si implantar un dispositivo como Neuralink conlleva el riesgo de causar daño al tejido cerebral, sería razonable suponer que retirarlo también lo hace.
Una definición de ‘abandono de dispositivo neurológico implantado’
Para fundamentar su estudio, los investigadores revisaron artículos sobre el abandono de dispositivos neurológicos antes de llegar a un consenso sobre una definición adecuada. Proponen la adopción de una definición estándar, que comprenda uno de los siguientes:
- No proporcionar información relevante a (la existencia o ausencia de) planes de responsabilidad médica, técnica y/o financiera como aspectos fundamentales del consentimiento del paciente durante y después de un ensayo clínico.
- No cumplir con la responsabilidad razonable de soporte médico, técnico y/o financiero antes del final de la vida útil indicada en la etiqueta de un dispositivo implantable.
- No abordar cualquier necesidad inmediata (por ejemplo, infección o reprogramación del dispositivo) del individuo que utiliza el dispositivo implantado, lo que puede resultar en problemas de seguridad y/o el deterioro de la efectividad del dispositivo.
- Fracaso de un ensayo de investigación clínica si o cuando (1) el consentimiento informado no ha abordado el acceso continuo y la gestión del dispositivo implantado (según 1, arriba) y/u otros dispositivos que puedan demostrar que tienen un valor terapéutico igual o mayor en el futuro y (2) las personas responsables del ensayo no han hecho un esfuerzo razonable para facilitar el acceso continuo al dispositivo y el soporte para los pacientes que se benefician del dispositivo.
Las cuestiones planteadas en este artículo dejan claro que se necesita una orientación mayor y más consistente en este campo en rápida evolución para proteger a los pacientes y a sus profesionales médicos.
«Opinamos que estos principios enumerados anteriormente pueden proporcionar una base de trabajo para una mayor consideración, discurso y diálogo hacia el establecimiento de una definición formal de abandono de dispositivos neurotecnológicos implantables activos y pautas, políticas y leyes para prevenir su ocurrencia», dijeron los investigadores.
El estudio fue publicado en la revista Red JAMA abierta.





