Al colocar «mochilas» de micropartículas en importantes células inflamatorias llamadas macrófagos, los investigadores redujeron significativamente el tamaño de la lesión y la inflamación causada por una lesión cerebral traumática. Al trabajar con la biología y no en contra de ella, este novedoso enfoque tiene el potencial de ser un tratamiento eficaz para una afección debilitante.
A nivel mundial, en 2019, hubo 27,16 millones de nuevos casos de lesión cerebral traumática (TBI) y 48,99 millones de casos de personas con TBI existentes. Si bien la neuroinflamación es importante para promover la regeneración de células y tejidos inmediatamente después de una lesión cerebral traumática, la inflamación prolongada puede provocar una lesión secundaria. La activación de los macrófagos residentes en el cerebro (glóbulos blancos que pueden cambiar entre estados proinflamatorios y antiinflamatorios) y otras células inmunitarias puede expandir la lesión y aumentar la probabilidad de complicaciones como depresión, déficits sensoriomotores y de memoria, y demencia.
Ahora, investigadores del Instituto Wyss de la Universidad de Harvard han reclutado macrófagos para ayudar en el tratamiento de la lesión cerebral traumática. Equipados con una “mochila” de micropartículas llena de moléculas antiinflamatorias, los macrófagos equipados redujeron significativamente la inflamación cerebral local, el tamaño de las lesiones y el sangrado en cerdos con TBI.
«Cada año, millones de personas sufren una lesión cerebral traumática, pero actualmente no existe ningún tratamiento más allá de controlar los síntomas», afirmó Samir Mitragotri, uno de los autores correspondientes del estudio. “Hemos aplicado nuestra tecnología de mochila celular, que anteriormente usábamos para mejorar respuesta inflamatoria de los macrófagos a tumores cancerosos, para administrar un tratamiento antiinflamatorio localizado en el cerebro, que ayuda a mitigar la cascada de inflamación descontrolada que causa daño tisular y la muerte en un modelo relevante para los seres humanos”.
A medida que las células cerebrales mueren debido a un impacto traumático, liberan un cóctel de citocinas proinflamatorias que atraen a las células inmunitarias para reparar el daño. Pero estas citocinas también pueden alterar la barrera hematoencefálica, provocando que la sangre se filtre al cerebro, lo que provoca hinchazón, alteración del suministro de oxígeno y aumento de la inflamación. Es un círculo vicioso de hemorragia y daño que provoca aún más muerte celular.
Basándose en su trabajo anterior adaptando mochilas a macrófagos, los investigadores pensaron que podrían ser eficaces en casos de TBI.
«En general, se cree que las terapias antiinflamatorias pueden ser efectivas para tratar la lesión cerebral traumática, pero, hasta ahora, ninguna de ellas ha demostrado ser efectiva clínicamente», dijo Rick Liao, coautor principal del estudio. “Nuestro trabajo anterior con macrófagos nos ha demostrado que podemos utilizar nuestra tecnología de mochila para dirigir eficazmente su comportamiento cuando llegan al lugar de la lesión. Dado que estas células ya son actores activos en la respuesta inmune natural del cuerpo a una lesión cerebral traumática, teníamos la corazonada de que podíamos aumentar esa biología preexistente para reducir el daño inicial”.
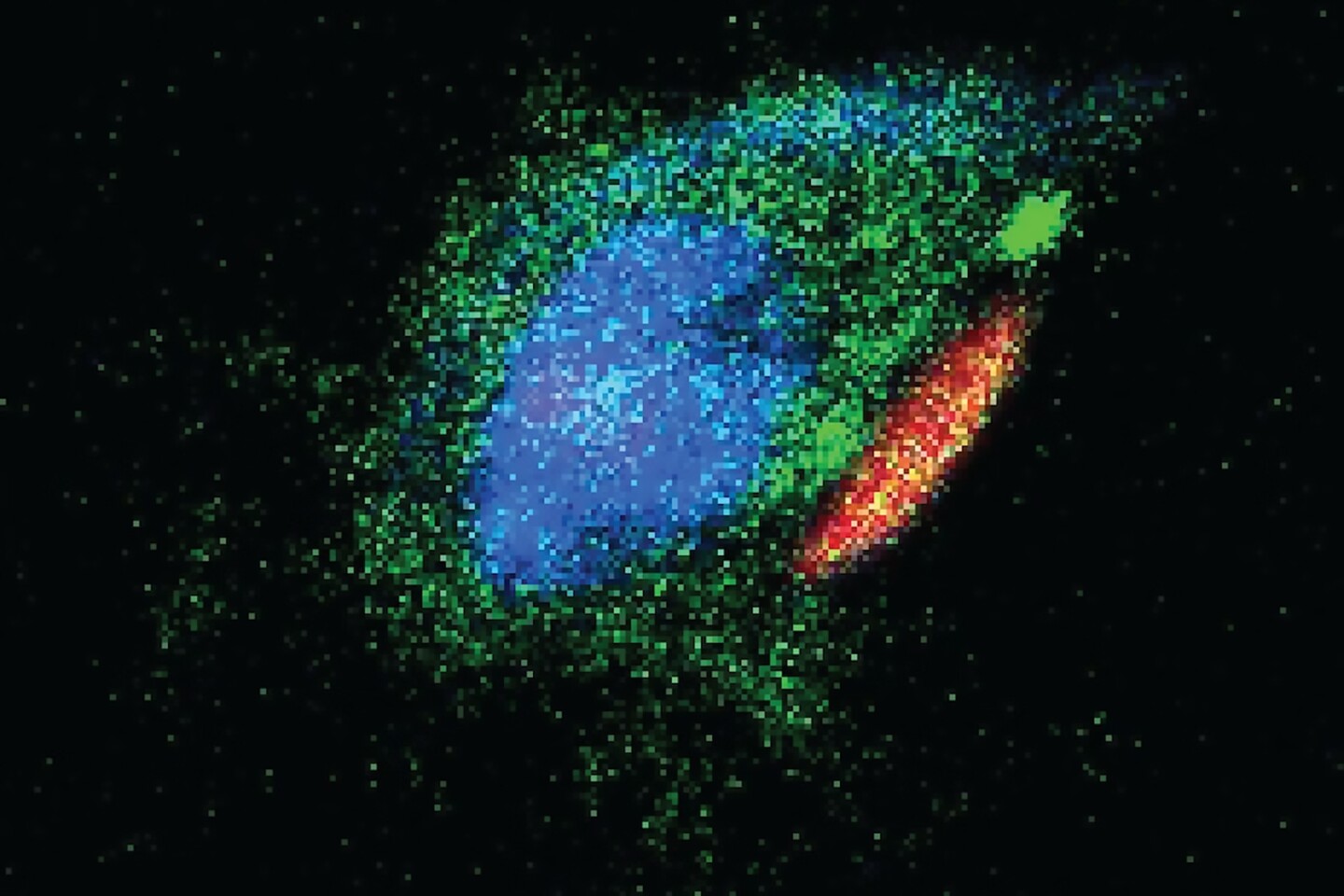
Instituto Wyss de la Universidad de Harvard
Las mochilas celulares se componen de dos capas externas de dexametasona, un medicamento esteroide antiinflamatorio, en poli(ácido láctico-co-glicólico) (PLGA) y una capa intermedia de IL-4, una citoquina inmunorreguladora, en poli(alcohol vinílico). ) (PVA). Se ha demostrado que la combinación de dexametasona e IL-4 induce un efecto antiinflamatorio sinérgico. Las mochilas tienen un diámetro promedio de 8,2 µm y un espesor de 914 nm y están diseñadas para adherirse a la superficie de los macrófagos.
Se cultivaron macrófagos de cerdo a partir de médula ósea y se les colocaron mochilas para crear un complejo mochila-macrófagos. Los complejos se administraron por vía intravenosa a modelos porcinos de TBI con una lesión en la corteza, la capa más externa del tejido cerebral. Siete días después, se observaron macrófagos en mochila en la lesión lesionada en mayor densidad que en otras áreas del cerebro.
En comparación con los cerdos que recibieron una inyección de solución salina, el tratamiento con macrófagos de mochila redujo el volumen total de la lesión macroscópica en un 56% y produjo una reducción «visualmente sorprendente» en la cantidad de hemorragia (73 mm3 frente a 21 mm3). El volumen de hemorragia se correlacionó positivamente con el volumen de la lesión, lo que indica que se vio muy afectado por la cantidad de hemorragia de la lesión a medida que evolucionaba. Los macrófagos de mochila redujeron el volumen de la lesión microscópica, una evaluación del daño tisular permanente, en un 47%. También se observó que los cerdos tratados con las mochilas tenían menos lesiones grandes.

Instituto Wyss de la Universidad de Harvard
Los investigadores analizaron la microglia, las células reparadoras de lesiones del cerebro, en las lesiones de los cerdos tratados y encontraron una reducción en el marcador proinflamatorio CD80 en comparación con el grupo de solución salina. Los biomarcadores periféricos de inflamación también fueron menores en los cerdos tratados con macrófagos de mochila. Veinticuatro horas después de la lesión, el factor de necrosis tumoral alfa (TNF-⍺), un importante regulador de las respuestas inflamatorias, era del 82,7% en los cerdos tratados en comparación con el 117,5% en los controles. Siete días después de la lesión, la proteína ácida fibrilar glial sérica (GFAP), un biomarcador de diagnóstico y pronóstico de TBI y neuroinflamación, fue menor en los grupos tratados (75,2%) versus solución salina (158,4%).
La tasa de eventos adversos para los cerdos tratados no difirió de la de los animales que recibieron solución salina. No se observaron signos de toxicidad debido al tratamiento con macrófagos de mochila en el bazo, el hígado, los riñones y los pulmones.
«La susceptibilidad de los macrófagos a su entorno local ha impedido históricamente que los científicos aprovechen al máximo sus capacidades de modulación inmunológica», dijo el director fundador del Instituto Wyss, Donald Ingber, que no participó en la investigación. «Este impresionante estudio describe una terapia basada en macrófagos verdaderamente novedosa y potencialmente poderosa para tratar la inflamación que es la causa fundamental de tantas enfermedades humanas de una manera efectiva y no invasiva que trabaja con la biología en lugar de contra ella».
El estudio fue publicado en la revista Nexo PNAS.
Fuente: Instituto Wyss de Harvard