Es posible que el tejido cerebral dañado vuelva a crecer utilizando un nuevo método que permite a los investigadores guiar las células madre hacia exactamente el tipo de células cerebrales que necesitan para un lugar en particular. Están apuntando a nuevos tratamientos para los accidentes cerebrovasculares, las lesiones cerebrales traumáticas y la EM.
El cerebro y la médula espinal tienen una capacidad limitada para regenerarse después de una lesión. Después de una lesión primaria causada por un derrame cerebral, una lesión cerebral traumática o una lesión de la médula espinal, la inflamación y la formación de tejido cicatricial causan un daño tisular secundario que es difícil de curar.
La reparación de una lesión cerebral utilizando células madre neurales o progenitoras, que pueden autorrenovarse y diferenciarse en células cerebrales específicas como neuronas y células gliales, es muy prometedora. Sin embargo, las células madre deben llegar al tejido en un medio que garantice su supervivencia y posterior crecimiento.
Investigadores de la Universidad Ruhr de Bochum y la Universidad de Dortmund en Alemania han desarrollado un medio de hidrogel cargado positivamente que guía la diferenciación de las células madre neurales en células particulares que podrían ayudar a regenerar el tejido cerebral lesionado.
«Nuestro objetivo era crear un entorno artificial para las células que imitara el entorno celular natural del cerebro», dijo Kristin Glotzbach, autora principal del estudio. “Las células tienen una capa cargada negativamente, también llamada matriz pericelular. Esto significa que se adhieren particularmente bien a sustratos cargados positivamente”.
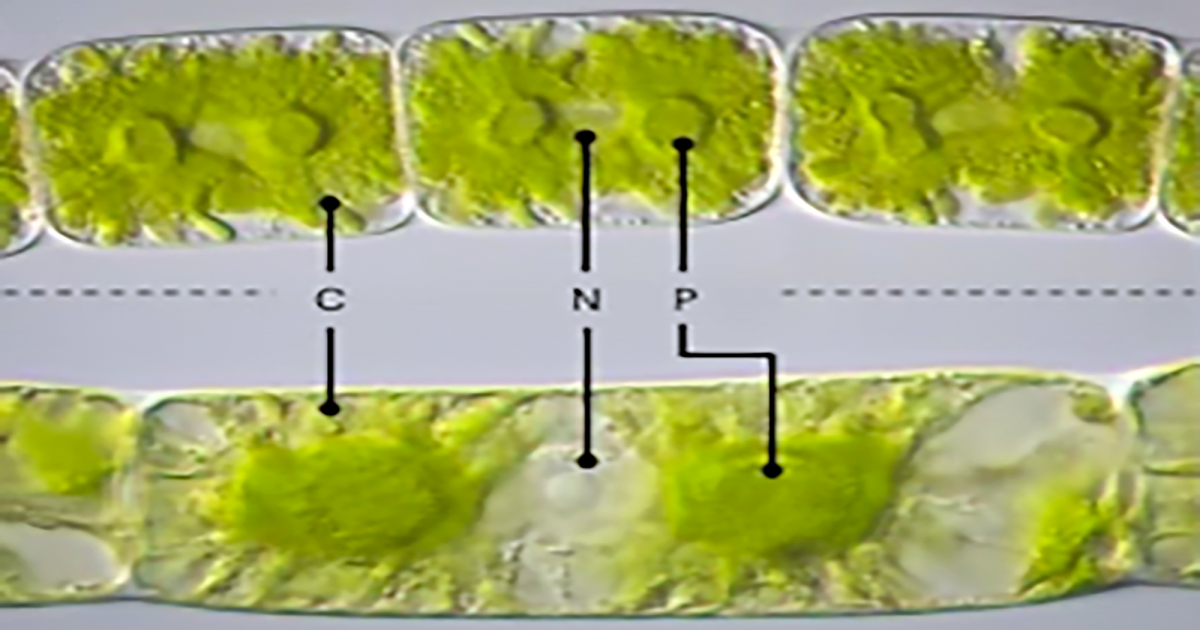
Las células madre neurales pueden diferenciarse en tres tipos de células: neuronas, astrocitos y oligodendrocitos. Las neuronas son las unidades fundamentales del cerebro y del sistema nervioso, responsables de recibir información sensorial del mundo exterior, enviar órdenes motoras a los músculos y transformar y transmitir señales eléctricas en cada paso intermedio. Los astrocitos y oligodendrocitos son subtipos de células gliales que brindan soporte, conectan y protegen a las neuronas.
El uso de hidrogeles como medio para células madre no es algo nuevo. Pero relativamente pocos investigadores han utilizado hidrogeles catiónicos o cargados positivamente. Entonces, para el estudio actual, los investigadores se propusieron sintetizar uno. La clave fue la molécula catiónica acrilato de trimetilaminoetilo (TMAEA); con él, crearon seis geles (G1 a G6) con concentraciones crecientes de carga catiónica. G1 no estaba cargado y actuó como gel de referencia neutro.
Utilizando células madre neurales y progenitoras (NSPC) de cerebros embrionarios de ratón, los investigadores colocaron 40.000 células en cada uno de los seis hidrogeles. Descubrieron que la carga catiónica del gel influía mucho en la diferenciación de las células. El G5, el segundo hidrogel con mayor carga positiva, tenía significativamente más neuronas que el G1 sin carga. Por el contrario, los hidrogeles G2 y G3 con menor carga albergaban significativamente más astrocitos que el G6 con alta carga. El mayor número de oligodendrocitos se encontró en G1, G3 y G4 y el más bajo en G6, pero en general, el porcentaje de oligodendrocitos fue significativamente menor en comparación con las neuronas y los astrocitos. En conjunto, los perfiles de diferenciación celular de los hidrogeles G1 a G6 mostraron que cada tipo de célula respondía mejor a una determinada concentración de carga catiónica.
Si bien las NPSC sobrevivieron con los hidrogeles catiónicos, los investigadores descubrieron que agregar el factor de crecimiento de fibroblastos 2 (FGF2), que regula muchas funciones celulares en el cuerpo, incluida la proliferación y diferenciación celular, aumentaba la supervivencia y la tasa de división de las células.
Ser capaz de guiar a las células madre para que se diferencien en células cerebrales específicas tiene ventajas, dicen los investigadores.
«Dependiendo de la lesión, es necesario reemplazar diferentes tipos de células», dijo Glotzbach. “En determinadas enfermedades, también se atacan las células gliales, que luego se quieren reemplazar. Por ejemplo, en la esclerosis múltiple se destruye el aislamiento de las células nerviosas, formado por los oligodendrocitos».
Los investigadores planean continuar perfeccionando su hidrogel, incluido el desarrollo de un gel que pueda usarse para llenar cavidades en el tejido cerebral después de una lesión.
«En futuros estudios nos gustaría equipar los geles cargados positivamente con péptidos o componentes de moléculas de la matriz extracelular y así estimular aún mejor el entorno natural de las células», afirma Glotzbach.
El estudio fue publicado en la revista ACS Biomateriales Ciencia e Ingeniería.
Fuente: Universidad del Ruhr en Bochum